Impact de l’étalement au râteau sur le dénombrement des microorganismes
« Personne n’aime prendre un râteau sauf peut-être les… microbiologistes ! »
Don Juan
Qu’on le nomme râteau, étaleur, spatule, le truc en L pour étaler ou le râteau de Drigalski (le débat est encore ouvert sur LinkedIn), l’utilisation de cet instrument doit être maitrisé à la perfection !
Une utilisation trop intensive et on risque de perdre tuer des microorganismes, une utilisation trop « laxiste » et le dénombrement sera impossible !
Bref ratisser n’est pas une action anodine.
Qu’est-ce que le râteau de Drigalski ?

La spatule de Drigalski fut inventé par… Wilhelm von Drigalski (un bactériologiste allemand). A l’origine, les spatules étaient composées en verre ou en métal. Elles étaient constituées d’un manche et d’une partie en forme de triangle (en contact avec la gélose).
Aujourd’hui les râteaux ont plutôt une forme de L et sont fabriqués en plastique. Certains laboratoires de microbiologie les fabriquent eux-mêmes en chauffant une pipette Pasteur… et oui les microbiologistes peuvent aussi être de formidables sculpteurs sur verre.
Au final, peu importe la forme ou le nom, l’utilisation reste la même.
Le râteau est un outil utilisé par les microbiologistes non pas pour jardiner (quoique) mais pour étaler une solution de microorganismes à la surface d’une gélose. Lors de l’étalement le liquide pénètre dans la gélose ce qui permet une répartition homogène des microorganismes. Cette manipulation permet de faciliter l’énumération des microorganismes.
Parce que oui l’objectif principal du râteau est de pouvoir compter les microorganismes présent dans l’échantillon de départ.
Les Meilleures Souches
Découvrez les meilleures marques de souches pour le Pharma
Nous avons sondé les SuperMicrobiologistes.
Voici leurs souches préférées
Attention à la durée de l’étalement
Une étude mené par Hedderich et al* a montré que la durée de l’étalement pouvait avoir une incidence sur la viabilité de certaines souches, notamment celle des bactéries à Gram négatifs.
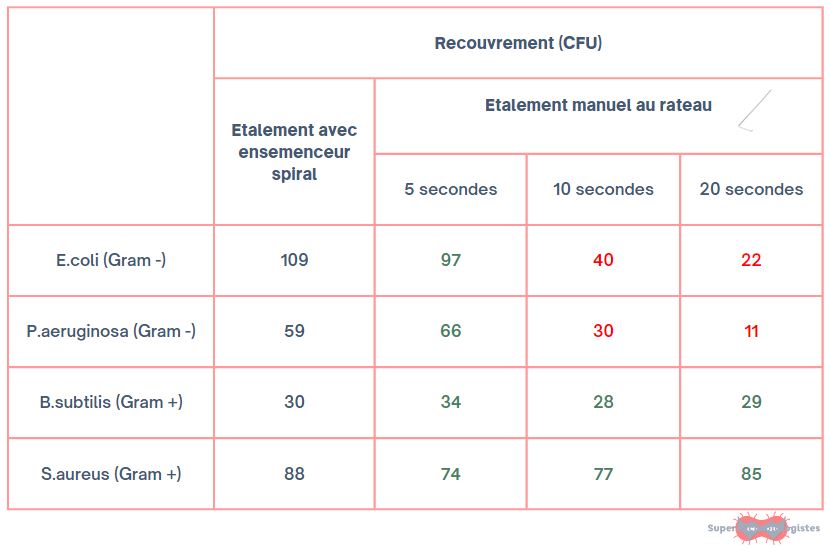
On remarque qu’on perd 50 % des bactéries à Gram négatif (Escherichia coli et Pseudomonas aeruginosa) après 10 secondes d’étalement et 80% après 20 secondes. Ça chamboule, non ?!
Les chercheurs ont ensuite observé l’état des microorganismes avec un microscope électronique
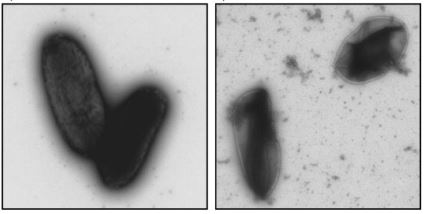
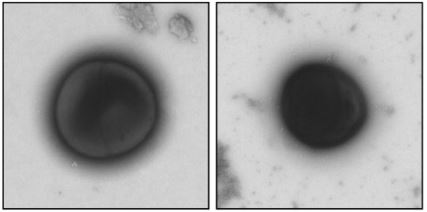
Les observations au microscope électronique montre bien que l’étalement au râteau endommagent fortement les membranes des bactéries à Gram négatif. Par contre cette même manipulation n’a pas le même effet sur la membrane des bactérie à Gram positif.
Les Meilleures Souches
Découvrez les meilleures marques de souches pour l’Agroalimentaire et l’Hydrologie
Nous avons sondé les SuperMicrobiologistes.
Voici leurs souches préférées
Conclusion
« Que ça soit pour les tests de fertilité ou pour les analyses d’énumération de routine, il faut y aller mollo sur le râteau. »
En plus de challenger les milieux de culture, les tests de fertilité peuvent permettent de se rendre compte d’un problème de manipulation au niveau du laboratoire de microbiologie… et dans notre cas particulier d’un problème d’étalement au râteau.
Si lors de vos tests de fertilité vous avez régulièrement des problèmes de recouvrement pour vos bactéries à Gram négatif c’est peut-être à cause de la durée de l’étalement. Après investigation, si l’étalement est effectivement en cause, il faudra revoir les procédures internes pour standardiser cette étape en la limitant à 5 secondes ou à 5 « coups de râteau par exemple.
Mais le plus important reste d’en discuter avec vos collègues microbiologistes pour connaitre leurs pratiques et éventuellement les alerter sur cette problématique encore peu connue.
* Hedderich, R., Müller, R., Greulich, Y., Bannert, N., Holland, G., Kaiser, P., Reissbrodt, R. Mechanical damage to Gram-negative bacteria by surface plating with the Drigalski-spatula technique
(2011) International Journal of Food Microbiology, 146 (1), pp. 105-107.
A la lecture de cet article, si vous avez des objections ou des questions complémentaires, venez alimenter le débat en laissant un commentaire ci-dessous.
Pour ne pas louper le prochain article, inscrivez-vous à la newsletter ici !









Merci pour ce bel article. Très intéressant, simple et efficace… comme toujours
Qu en est il de l étalement avec des billes? Ce serait l occasion de comparer les deux types avec un temps défini
C’est une bonne question Anne, nous allons creuser 😉 !
Bonjour,
merci très intéressant. A la vue du tableau, je me dis que c’est cool pour les étalement effectués en labo de routine. Majoritairement des Gram + ( Staph et Bacillus). Donc un étalement de 15 à 20 s ( la norme dit jusqu’à absorption de l’inoculum, on doit récupérer la totalité des germes et avoir une meilleure sélectivité avec la flore interférente ( gram -) ?? Finalement la norme est ok 😉 ??
Muriel,
Merci pour votre commentaire.
Il serait intéressant de savoir si ce genre de publication a été pris en compte pour faire la norme (même s’il n’y a pas de « durée » dans la norme). Il s’agit bien évidement d’un compromis entre un étalement trop long (mortel pour les G-) et un étalement trop court (illisible).
Dans les faits, on a tout de même l’impression que les étalements ne durent pas plus de 15 secondes… c’est long 15 secondes 😉 !
J’en conclu que des coups de râteau de 20secondes sur mon steak haché reduit le risque de toxi infection à E. coli ! Intéressant ☺️ Merci beaucoup pour ces informations plus qu’intéressantes et importantes à connaître!
Ahah, très intéressant, dommage qu’il n’y ait pas le résultat sans étalement.
En effet, cela facilite le dénombrement, quand on s’attend à avoir un haut niveau de détection.
Est-ce vraiment utile pour l’analyse du stérile ou d’échantillons relativement propres?
Bonjour Saralstonia (très bon jeu de mot !)
Le râteau est et reste très pratique, par contre il faut savoir l’utiliser avec parcimonie… pas plus de 5 secondes 😉